 |
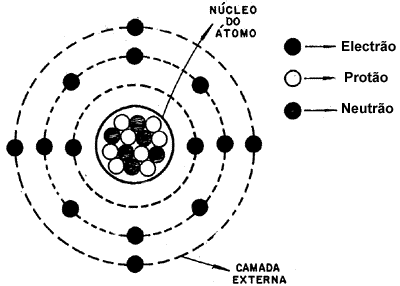
Figura 1 - Representação esquemática de um átomo genérico |
| Semicondutores |
Os dispositivos semicondutores (díodos, transístores, diacs, triacs, mosfet,
circuitos integrados, etc) constituem, sem dúvida alguma, uma verdadeira revolução
no campo da tecnologia dos componentes electrónicos. Estes minúsculos
componentes realizam praticamente todas as tarefas que antes eram confiadas às
válvulas electrónicas, porém com muito mais eficácia e segurança.
Enquanto que o princípio de uma válvula electrónica se baseia no fluxo de electrões que há do cátodo para a placa, através do vácuo existente no interior do invólucro de vidro que constitui a válvula, enquanto que o princípio de funcionamento dos dispositivos semicondutores, apesar de também basear-se num fluxo de electrões, se realiza em material sólido (geralmente silício ou germânio), e não no vácuo, como nas válvulas electrónicas. Por esta razão, os dispositivos semicondutores são também denominados dispositivos de estado sólido.
Constituição da matéria
As substâncias encontradas na natureza, sejam elas sólidas, líquidas ou
gasosas, são constituídas por um aglomerado de minúsculas partículas,
chamadas moléculas, que são a menor parte que se pode obter de uma substância,
conservando as mesmas características e propriedades (ponto de fusão,
resistividade eléctrica, massa especifica, etc.). Se tivermos uma gota de água
e a dividirmos, sucessivamente, em diversas partes, a menor delas, que ainda
conserva as características da gota inicial, será a molécula de água.
 |
Figura 1 - Representação esquemática de um átomo genérico |
As moléculas podem ainda ser subdivididas em partículas menores que são os átomos; contudo, estas novas partículas já não apresentam as mesmas propriedades da substância original. Assim subdividirmos uma molécula de água, obteremos três partículas, sendo duas iguais entre si (átomos de hidrogénio) e a terceira diferente (átomo de oxigénio). Concluímos que a molécula da substância água (H2O) é constituída por dois átomos de hidrogénio (H) e um de oxigénio (O).
Estrutura do átomo
O átomo (a menor partícula constituinte da matéria) é uma palavra de origem grega e significa não divisível. Este nome lhe foi dado por ocasião da sua descoberta, quando realmente se pensava que fosse impossível dividi-lo. Entretanto, através das modernas teorias da Física Nuclear, hoje sabemos que o átomo e basicamente formado por três tipos de partículas elementares: electrões, protões e neutrões. Destas, os protões e os neutrões formam a sua parte central (núcleo), ao redor da qual giram os electrões, em altíssimas velocidades. A carga do electrão é igual à carga do protão, porém de sinal contrário; o electrão possui carga negativa (-) e o protão carga eléctrica positiva (+). O neutrão não possui carga eléctrica, isto e, sua carga é nula.
Num átomo, os electrões que giram ao redor do núcleo distribuem-se em várias regiões (camadas), num total de 7. Na figura 1 temos a representação esquemática de um átomo genérico.
Todos os elementos encontrados na Natureza são formados por diferentes tipos de átomos, diferenciados entre si pelos seus números de protões, electrões e neutrões. A Tabela 1 mostra a constituição de alguns elementos químicos (tipos de átomos) conhecidos até hoje.
Analisando a Tabela, concluímos: em qualquer átomo, o número de protões contidos no seu núcleo é igual ao número de electrões que giram ao redor dele.
Tabela I |
||||
| Nome do Elemento | Símbolo Químico | Número de Protões | Número de Electrões | Número de Neutrões |
| Hidrogénio |
H |
1 |
1 |
0 |
| Hélio |
He |
2 |
2 |
2 |
| carbono |
C |
6 |
6 |
6 |
| Sódio |
Na |
11 |
11 |
12 |
| Alumínio |
Al |
13 |
13 |
14 |
| Silício |
Si |
14 |
14 |
15 |
| Cloro |
Cl |
17 |
17 |
18 |
| Germânio |
Ge |
32 |
32 |
41 |
| Prata |
Ag |
47 |
47 |
61 |
| Antimônio |
Sb |
51 |
51 |
71 |
| Tungstênio |
W |
74 |
74 |
110 |
| Ouro |
Au |
79 |
79 |
118 |
| Mercúrio |
Hg |
80 |
80 |
120 |
| Urânio |
U |
92 |
92 |
136 |
IÕES POSITIVOS E IÕES NEGATIVOS
Quando um átomo perde um ou mais electrões, dizemos que ele se transforma num ião positivo
. Consideremos o átomo de Sódio (Na), que possui 11 protões e 11 electrões. No caso de perder 1 electrão, ele ficará com 11 protões e 10 electrões, resultando: (+11) + (-10) = +1, o que indica que o átomo de Sódio não é mais neutro, já que ele apresenta uma carga eléctrica positiva, igual à do protão. Temos assim, o ião positivo de sódio.CAMADA DE VALÊNCIA E ELECTRÕES DE VALÊNCIA
Como já mencionamos, os electrões giram ao redor do núcleo em regiões
(num total de 7) que recebem o nome de camadas. Em todo átomo, a camada mais
afastada do núcleo (camada externa, figura 1), é a camada de valência, e os
electrões dessa camada são chamados de electrões de valência. Eles tem uma
função muito importante pois, na maioria das vezes, são eles que participam
das reacções químicas e dos fenómenos eléctricos.
Na Tabela II ilustramos o número de electrões de valência de alguns elementos
químicos. Os átomos com 1, 2 e 3 electrões de valência têm uma certa
facilidade em cedê-los, transformando - se em iões positivos; o alumínio
(Al), o cálcio (Ca), o Sódio (Na) ,etc., são alguns exemplos.
Os átomos com 5, 6 e 7 electrões de valência têm facilidade em ganhar electrões,
transformando-se em iões negativos; o fósforo (P), o oxigénio (O), o cloro
(Cl), etc, estão neste caso.
Os átomos com 4 electrões de valência geralmente não ganham nem perdem electrões, é o que ocorre com o Carbono (C), o Silício (Si), o Germânio (Ge), etc.
Tabela II |
||
| Nome do Elemento | Símbolo Químico | Electrões de Valência |
| Sódio |
Na |
1 |
| Cálcio |
Ca |
2 |
| Alumínio |
Al |
3 |
| Boro |
B |
3 |
| Gálio |
Ga |
3 |
| Índio |
In |
3 |
| Carbono |
C |
4 |
| Silício |
Si |
4 |
| Germânio |
Ge |
4 |
| Antimônio |
Sb |
5 |
| Arsénio |
As |
5 |
| Fósforo |
P |
5 |
| Oxigénio |
O |
6 |
| Cloro |
Cl |
7 |
LIGAÇÕES QUÍMICAS
A maneira pela qual os átomos se unem para formar a molécula de uma
substância recebe o nome de ligação química, ou simplesmente ligação.
Ao juntarmos um átomo de Sódio (Na) com um átomo de Cloro (Cl), inicialmente
neutros, verificamos que o átomo de Cloro "rouba" um electrão (o de
valência) do átomo de Sódio, transformando o átomo de Cloro num ião
negativo (ganhou 1 electrão), e o de Sódio num ião positivo (perdeu 1 electrão).
Como cargas eléctricas de sinais contrários (+ e -) se atraem, os iões de
Cloro e Sódio são atraídos entre si, formando a molécula de Cloreto de Sódio
(NaCl), vulgarmente conhecida como sal de cozinha. Este processo recebe o nome
de Ligação iônica e está representado na figura 2.
Figura 2 - Representação esquemática da ligação iônica
Outro tipo de ligação é a que ocorre entre átomos de hidrogénio, quando eles se unem para formar a molécula do gás Hidrogénio (H2) , onde nenhum átomo perde ou ganha electrões, havendo apenas um "empréstimo". Um átomo empresta o seu electrão e toma emprestado o electrão do outro, formando, assim, uma espécie de "sociedade", em que os dois átomos "compartilham" de seus electrões. Esta é a chamada ligação covalente, que está ilustrada na figura 3.
Figura 3 - Representação esquemática da ligação covalente
A ligação covalente tem uma importância muito grande para o estudo que ora iniciamos, pois é nela que estão as características dos materiais semicondutores utilizados na fabricação dos dispositivos de estado sólido.
De um modo geral, todas as substâncias existentes na Natureza têm os seus átomos unidos por um desses tipos de ligação.
CONDUTORES, ISOLANTES E SEMICONDUTOPES
Tabela III |
|
| Substância | Resistividade (W x cm) |
| Prata | 1.6 x 10-6 |
| Cobre | 1.7 x 10-6 |
| Ouro | 2.3 x 10-6 |
| Alumínio | 2.8 x 10-6 |
| Tungsténio | 4.9 x 10-6 |
| Grafite | 6 x 10-3 |
| Germânio (puro) | 47 |
| Silício (puro) | 21.4 x 104 |
| Vidro | 1012 |
| Porcelana | 3 x 1014 |
| Baquelita | 2 x 1016 |
| Borracha | 9 x 1016 |
| Mica | 1017 |
CONDUTORES - São materiais que possuem uma
resistência muito baixa, não oferecendo, praticamente,
nenhuma oposição à
passagem da corrente eléctrica. A prata, o chumbo, o alumínio, etc, são
exemplos desses condutores.
Num material condutor os electrões de valência são atraídos pelo núcleo
dos átomos, com uma força muito fraca, encontrando uma grande facilidade para
abandonar seus átomos e se movimentarem "livremente" no interior da
substância. Por esse motivo é que eles são chamados "electrões livres".
ISOLANTES - São materiais que possuem uma
resistividade muito alta, bloqueando a passagem da corrente eléctrica. O vidro,
a mica, a borracha, etc, estão neste caso.
Num material isolante, os electrões de valência estão rigidamente ligados ao
núcleo dos átomos, sendo que pouquíssimos electrões conseguem desprender-se
de seus átomos para se transformarem em electrões livres.
Na figura 4 está Ilustrada uma experiência que permite observar a diferença existente entre um condutor e um isolante. A figura 4A mostra uma pilha seca, ligada em série com uma barra de material condutor (Cobre), tendo Intercalado no circuito um medidor de corrente (amperímetro).
Figura 4 - Diferença entre um condutor (A) e um isolante (B)
O Cobre, sendo um condutor, possui um número
extremamente elevado de electrões livres, que são atraídos pelo polo positivo
da pilha seca, formando uma corrente eléctrica multo intensa que será
detectada pelo medidor. Na figura 4B, a barra de Cobre é substituída por uma
barra de material isolante (vidro). Como este tipo de material possui um número
extremamente reduzido de electrões livres, a corrente eléctrica que atravessa
o circuito e é detectada pelo medidor, pode ser considerada como igual a zero.
SEMICONDUTORES - Materiais que apresentam uma resistividade Intermediária,
isto é, uma resistividade maior que a dos condutores e menor que a dos
isolantes. Como exemplo, podemos citar o Carbono, o Silício, o Germânio, etc.
Com referência à condução da corrente eléctrica, os semicondutores a
conduzem mais que os isolantes, porém menos que os condutores. Isto pode ser observado
na experiência mencionada anteriormente, se ligarmos uma barra de material semicondutor
(Silício) em série com o circuito (figura 5).
Figura 5 - O semicondutor comporta-se de um modo intermédio entre o isolante e o condutor
Para diferenciar um condutor, um isolante e um semicondutor, consideremos uma barra com 10 cm de comprimento e 1 cm2 de secção transversal ( figura 6). Se a barra for de Cobre, ela apresentara uma resistência da ordem de 17mW (0.000017W); se for de vidro, sua resistência será cerca de 10.000.000 MW; e, se for de Silício, ele será de aproximadamente 2,14 MW.
Em nosso estudo daremos maior desta que aos dois materiais semicondutores, Silício e Germânio, que são os mais usados na fabricação de dispositivos de estado solido.
Sabemos que o átomo de Germânio possui 32 electrões e portanto, é maior que o de Silício, em que há apenas 14 (figura 7). Ambos possuem 4 electrões de valência (veja a Tabela II)
, sendo, por esta razão chamados de átomos tetravalentes (tetra=quatro), e podem ser considerados semelhantes sob o ponto de vista eléctrico.A resistividade do Silício é bem maior que a do Germânio (Tabela III), porque o átomo de Silício, sendo menor que o átomo de Germânio, possui seus electrões de valência mais rigidamente ligados ao núcleo, tendo, desta maneira, menos e1ectrões livres, o que aumenta a sua resistividade.
EFEITO DA TEMPERATURA
Experimentalmente verifica-se que os condutores e os semicondutores comportam-se de maneira oposta em re1ação à temperatura. A resistividade dos condutores aumenta com a elevação da temperatura, enquanto que a resistividade dos semicondutores diminui.
Na figura 6 ilustramos uma barra de Cobre em cujo interior podemos imaginar os seus electrões livres num movimento contínuo e desordenado. Este movimento recebe o nome de movimento de agitação térmica. Fornecendo calor à barra, a temperatura aumentará, provocando uma agitação térmica maior e, consequentemente, muitas colisões entre electrões livres e átomos de Cobre. A oposição oferecida pelo material à passagem da corrente eléctrica será maior, acarretando o aumento da resistividade do Cobre. Os materiais semicondutores comportam-se de modo completamente oposto: à medida que a temperatura aumenta, a resistividade diminui.
Figura 6 - Barra com 10 cm de comprimento e 1 cm2 de secção transversal
ESTRUTURA CRISTALINA DOS SEMICONDUTORES
Quando os átomos se unem para formar as moléculas de uma substância, a distribuição desses átomos no espaço pode ou não ser feita organizada e definidamente. As substâncias cujos átomos se agrupam
formando uma estrutura ordenada são denominadas substâncias cristalinas, e a disposição de seus átomos formam a chamada estrutura cristalina. O Germânio e o Silício possuem uma estrutura cristalina cúbica, conforme é mostrado na figura 8.Figura 7 - Representação esquemática dos átomos de Germânio (Ge) e Silício (Si)
Nessa estrutura, cada átomo (representado por uma esfera escura) une-se a quatro outros átomos vizinhos, por meio de ligações covalentes, e cada um dos quatro electrões de valência de um átomo é compartilhado com um electrão do átomo vizinho, de modo que dois átomos adjacentes compartilham os dois electrões.
Além do Germânio e do Silício, há outros materiais semi
condutores cristalinos, bastante utilizados na fabricação dos dispositivos de estado sólido, tais como Arseneto de Gálio, Fosfeto de Gálio, Sulforeto de Cádmio, Carbeto de Silício, Sulfeto de Chumbo, etc.Figura 8 - Representação esquemática da estrutura cristalina do Germânio e do Silício
Devido à dificuldade de se representar a estrutura cristalina do Germânio e do Silício na sua forma espacial (figura 8), utilizaremos num mesmo plano. Portanto, os átomos de Germânio e de Silício serão representados numa maneira simplificada (figura 9), onde mostramos apenas os 4 electrões de valência (bolinhas pretas) ao redor de um circulo (núcleo + electrões restantes). Ainda na figura 9, temos as representações simplificadas do átomo de Índio ( que possui 3 electrões de valência) e também do átomo de Arsênio (5 electrões de valência), que serão utilizados mais adiante, quando tratarmos das impurezas. Nessa representação, supomos que todos os átomos são electricamente neutros (número de protões = numero de electrões) . Na figura 10 temos a estrutura cristalina do Silício, vista num único plano.
Convêm ressaltar que tudo o que foi dito para o Silício também se aplica ao Germânio pois, como já vimos, o Germânio e o Silício são átomos semelhantes sob o ponto de vista eléctrico.
ELECTRÕES E LACUNAS
Na prática, a estrutura cristalina ilustrada na figura 10 só é conseguida
quando o cristal de Silício é submetido à temperatura de zero graus absolutos
(ou -273ºC). Nessa temperatura, todas as ligações covalentes estão completas
e, consequentemente, o material comporta-se como isolante porque, não havendo
electrões livres, não será possível estabelecer uma corrente eléctrica
através do cristal.
Figura 9 - Representação simplificada dos átomos de Germánio (Ge); Silício (Si); Índio (In) e Arsénio (As)
Figura 10 - Estrutura cristalina planificada do Silício (-273º)
Quando este mesmo cristal de Silício é submetido à temperatura ambiente normal (200C, por exemplo), a energia térmica (calor) provoca o rompimento de algumas ligações covalentes, fazendo com que os electrões que abandonam as ligações rompidas passem a se movimentar livremente no interior do cristal, tornando-se electrões livres (figura 11).
Figura 11 - Estrutura cristalina do Silício à temperatura ambiente (20º)
Com a quebra das ligações covalentes, no local onde havia um electrão de valência (e), passa a existir uma região com carga positiva +1 (.), uma vez que o átomo de Silício era neutro e um electrão o abandonou. Essa região positiva que, em outras palavras, é uma ligação covalente incompleta, recebe o nome de LACUNA, sendo conhecida também como BURACO, CAVIDADE ou VAZIO.
Em síntese, à medida que a temperatura aumenta, surgem os "portadores
livres de carga eléctrica" (electrões e lacunas) no interior do cristal,
tornando-o capaz de conduzir corrente eléctrica quando submetido a uma
diferença de potencial. Isso explica o que foi dito anteriormente: "A
resistividade dos semicondutores diminui com a elevação de temperatura".
Sempre que uma ligação covalente é rompida, surgem, simultaneamente, um electrão
e uma lacuna, podendo, entretanto, um electrão preencher o lugar de uma lacuna,
completando a ligação covalente (processo da RECOMBINAÇÃO). Como tanto os electrões
como as lacunas sempre aparecem e desaparecem aos pares, dizemos então que, num
cristal semicondutor puro, o número de electrões livres é sempre igual ao número
de lacunas. A uma certa temperatura, o número de pares electrão-lacuna
é muito maior num cristal de Germânio puro que num cristal de Silício
pois, como já foi visto, a resistividade do Germânio é bem menor que a
resistividade do silício.
Figura 12 - No interior do cristal semicondutor, as lacunas movimentam-se em sentido contrário ao dos electrões
O MOVIMENTO DOS ELECTRÕES E DAS LACUNAS
A seguir mostraremos que a lacuna se comporta como se fosse uma partícula
semelhante ao electrão, porém com carga eléctrica positiva. Isto significa
que, quando o cristal é submetido a uma diferença de potencial (ou tensão eléctrica),
a lacuna pode mover-se do mesmo modo que o electrão, mas em sentido contrário,
uma vez que possui carga eléctrica a ele (figura 12 A).
Para compreender melhor esse movimento das lacunas, consideremos alguns átomos
de um cristal semicondutor (Silício ou Germânio), supondo que ele esteja
ligado aos pólos de uma pilha seca (figura 13). Se no átomo 1 for rompida uma
ligação covalente, aparecera um electrão, que será rapidamente atraído pelo
pólo positivo (+) da pilha seca (situação ilustrada na figura 13A), ficando
no lugar desse átomo uma lacuna. Um electrão de qualquer ligação covalente
do átomo 2 poderá preencher a lacuna deixada pelo primeiro electrão do átomo
1. Entretanto, quando o electrão abandona a ligação covalente do átomo 2,
surgirá uma nova lacuna (figura 13B) que, por sua vez, poderá ser preenchida
por qualquer electrão de uma ligação covalente do átomo 3 (figura 13C), e
assim sucessivamente.
Figura 13 - Representação esquemática do movimento dos electrões e das lacunas, quando o cristal semicondutor é submetido a uma diferença de potencial
Podemos concluir, então, que enquanto os electrões se
deslocam para a esquerda, em direcção ao pólo positivo da pilha seca (+), as
lacunas se deslocam para a direita, em direcção ao pólo negativo (-) da
pilha.
Outro fato importante refere-se à corrente eléctrica (1) que, pelo circuito
externo, é constituída apenas de electrões, que são atraídos pelo pólo
positivo, atravessam a pilha seca e são novamente injectados no material
semicondutor, através do pólo negativo da pilha. Invertendo a polaridade da
tensão aplicada no cristal (figura 12H), o sentido de deslocamento dos electrões
e das lacunas também será invertido.
Para finalizar, frisamos que as lacunas não têm existência real, pois são
apenas espaços vazios provocados pelos electrões que abandonam as ligações
covalentes rompidas. Contudo, utilizaremos o conceito de lacuna, porque ele será
muito útil para explicar o principio de funcionamento dos dispositivos de
estado sólido.
SEMICONDUTORES INTRÍNSECOS
Como já por diversas vezes citamos o termo CRISTAIS SEMICONDUTORES PUROS, vejamos, agora, o que isto significa, uma vez que na prática não se consegue uma pureza absoluta (100%).
O Silício e o Germânio são encontrados na própria Natureza, O Germânio é obtido de um pó branco, o Dióxido de Germânio, e o Silício é extraído do Oxido de Silício. Aquecendo-se o Dióxido de Germânio durante algumas horas, em uma atmosfera de Hidrogénio, obtém-se o Germânio metálico, já bastante puro, sob o ponto de vista químico.
Entretanto, para a fabricação de dispositivos semicondutores, exige-se um grau de pureza extremamente elevado (da ordem de 99,99999999%), que equivale a um grama de impurezas, no máximo, em cada 10.000 toneladas de material semicondutor. Portanto, quando nos referimos a um material semicondutor (como os ilustrados na figura 10 e 11) , estamos supondo que as impurezas contidas no cristal praticamente não interferem em seu comportamento eléctrico. A esse tipo de semicondutor, em que as impurezas nele existentes são apenas as que não puderam ser eliminadas durante o processo de purificação do cristal, damos o nome de SEMICONDUTOR INTRÍNSECO. Este termo significa que as características eléctricas do cristal são devidas ao próprio material semicondutor, e não às suas impurezas.
PROCESSO DE DOPAGEM - SEMICONDUTORES EXTRÍNSECOS
Há diversas maneiras de se provocar o aparecimento de electrões e lacunas livres no interior de um cristal semicondutor. Uma delas é através da energia térmica (ou calor), e a sua produção de pares, electrão-lacuna, recebe o nome de GERAÇÃO TÉRMICA DE PORTADORES. Outra maneira, consiste em fazer com que um feixe de luz incida sobre o material semicondutor, baseando-se este fenómeno no princípio de funcionamento dos DISPOSITIVOS FOTOSSENSÍVEIS. Na prática, contudo, necessitamos de um cristal semicondutor em que o número de electrões livres seja bem superior ao número de lacunas, ou de um cristal onde 5 número de lacunas seja bem superior ao número de electrões livres. Isto e conseguido tomando-se um cristal semicondutor puro (intrínseco) e adicionando-se a ele, por meio de técnicas especiais, uma determinada quantidade de outros tipos de átomos, aos quais chamamos de impurezas. Tais impurezas, propositadamente adicionadas ao cristal, têm uma concentração de cerca de um átomo par cada 1.000.000 átomos do material semicondutor. Damos a este processo o nome de DOPAGEM, termo proveniente da palavra inglesa "Doping", (substância estimulante, excitante, muito usada nos meios desportivos).
Quando são adicionadas impurezas a um cristal puro, este passa a ser impuro, sendo denominado, então, SEMICONDUTOR EXTRÍNSECO. Por extrínseco compreendemos que as características eléctricas do cristal se devem às impurezas a ele adicionadas, e não aos caracteres do próprio material.
A esta altura faz-se mister a seguinte pergunta: "- Por que, no início, o cristal é submetido a um rigoroso processo de purificação se, logo em seguida, são adicionadas impurezas? " A resposta é simples: As impurezas eliminadas inicialmente eram indesejáveis, porque não sabíamos o tipo e a quantidade das mesmas, não apresentando o cristal nenhuma aplicação útil . Contudo, após o processo de purificação, as impurezas adicionadas são do tipo conhecido e de quantidade bem detalhada, o que permite a fabricação de cristais semicondutores com características, para as mais diversas aplicações.
As impurezas utilizadas na "dopagem" de um cristal semicondutor podem ser de dois tipos: IMPUREZAS DOADORAS e IMPUREZAS ACEITADORAS.
IMPUREZAS DOADORAS - Tomemos como exemplo o átomo do elemento químico Arsénio(As), que possui 5 electrões na sua camada de valência, sendo, portanto, pentavalente (penta=cinco).
Por meio de um processo químico qualquer, conseguimos, substituir num cristal puro de Silício (Si), um de seus átomos por um átomo de Arsénio (As) (figura 14). Como este possui 5 electrões de valência, enquanto que o Silício apenas 4, somente 4 electrões de Arsénio participarão das ligações covalentes com os átomos de Silício. O quinto electrão, por não tomar parte nessas ligações será um electrão livre, podendo mover-se é vontade no interior do cristal, agindo como um "portador negativo de corrente eléctrica".
Figura 14 - Cristal semicondutor puro, onde átomo de Silício foi substituído por um átomo de Arsénio
Em síntese, a infiltração de átomos pentavalentes (como o Arsênio) num
cristal semicondutor puro, faz com que apareçam electrões livres no seu
interior. Como esses átomos fornecem (doam) electrões ao cristal semicondutor,
eles recebem o nome de IMPUREZAS DOADORAS. Todo cristal de Germânio ou Silício,
dopado com impurezas doadoras, é chamado de CRISTAL SEMICONDUTOR TIPO N (N
de negativo, referindo-se à carga
do electrão).
Outros átomos pentavalentes, usados como impurezas doadoras, são o
Antimônio (Sb) e o Fósforo (P).
IMPUREZAS ACEITADORAS
Vejamos agora o caso em que o átomo de Silício é substituído por um átomo de índio (In), conforme é ilustrado na figura 15. Como o índio é trivalente (possui 3 electrões na camada de valência), uma ligação covalente ficará incompleta. Nessa ligação haverá falta de um electrão, isto é, aparecerá uma lacuna; que será rapidamente preenchida por um electrão da ligação covalente com qual quer átomo vizinho, aparecendo no lugar desse electrão uma nova lacuna, e assim sucessivamente. Concluímos, então, que a lacuna provocada pelo átomo de índio ficará livre para se mover no interior do cristal, agindo como "portador positivo de corrente eléctrica".
Figura 15 - Cristal semicondutor puro, onde um átomo de Silício foi substituído por um átomo de Índio
Em síntese, a infiltração de átomos trivalentes (como o
Índio) num cristal
semicondutor puro: faz com que apareçam lacunas livres no seu interior. Uma vez
que esses átomos recebem (ou aceitam) electrões do cristal , eles são
denominados IMPUREZAS ACEITADORAS OU RECEPTORAS. Todo cristal puro dopado com
impurezas aceitadoras é chamado de CRISTAL SEMICONDUTOR TIPO P(P de positivo,
referindo-se a carga do protão).
Outros átomos trivalentes, usados como impurezas aceitadoras, são o Alumínio
(Ai), o Boro (B) e o Gálio (Ga).
Finalizando, convém salientar que, tanto no cristal tipo N como no tipo P, em
cada átomo o número de protões é igual ao número de electrões. Sendo
assim, o cristal impuro (tipo P ou N) é electricamente neutro.
PORTADORES MAJORITÁRIOS E PORTADORES MIN0RITÁRIOS
Num cristal semicondutor puro (cristal intrínseco) à temperatura ambiente,
aparecerão electrões e lacunas livres em igual número, devido à GERAÇÃO
TÉRMICA DE PORTADORES. Suponhamos que existam 100 pares de electrões-lacunas
(100 electrões e 100 lacunas livres), e que sejam adicionados átomos
pentavalentes (1.000, por exemplo). Como as impurezas doadoras (átomos
pentavalentes) fazem aparecer electrões livres no interior do cristal, cada
átomo de impureza doadora contribuindo com um electrão, teremos então 1000 electrões
livres, devido a tais impurezas. O cristal N, assim formado terá 100 lacunas e
1.100 electrões livres, na temperatura de 20ºC, como portadores de corrente eléctrica.
Notaremos, então, que teremos dois tipos de portadores nesse cristal.
Entretanto, devido ao fato de termos adicionado impurezas doadoras, fizemos com
que a maior parte dos portadores se transformassem em electrões.
Desta forma, num cristal semicondutor tipo N, os electrões são PORTADORES
EM MAIORIA ou PORTADORES MAJORITÁRIOS de corrente eléctrica. As lacunas, por
sua vez, são PORTADORES EM MINORIA ou PORTADORES MINORITÁRIOS de corrente eléctrica.
Se no cristal intrínseco forem adicionados átomos trivalentes (1.000, por
exemplo), cada um desses átomos (impureza aceitadora) contribuirá com uma
lacuna; teremos, então, 1.000 lacunas livres provocadas por tais impurezas. O
cristal tipo P, assim formado, terá 100 electrões e 1.100 lacunas livres como
portadores da corrente eléctrica, à temperatura de 20ºC. Assim sendo no
cristal P os portadores MAJORITÁRIOS são lacunas, pois estão em rnaioria é
os portadores MINORITÁRIOS são os electrões, que constituem a minoria.
Na Tabela IV temos um resumo de tudo quanto foi exposto sobre o comportamento das impurezas.
Para finalizar, suponhamos que o cristal tipo N ou o tipo P sejam submetidos à temperatura de zero grau absoluto (-273ºC) , quando os 100 electrões e as 100 lacunas, gerados termicamente, irão desaparecer (fenómeno da RECOMBINAÇÃO), ficando apenas os 1.000 electrões livres e as 1.000 lacunas produzidas pelas impurezas. Isto permite concluir que, enquanto o cristal puro (intrínseco) é um isolante perfeito, à temperatura de -273ºC, o cristal impuro (extrínseco) não apresenta esse isolamento à mesma temperatura.
MOVIMENTO DOS ELECTRÕES E DAS LACUNAS NOS SEMICONDUTORES
DOPADOS
Num cristal tipo N, o fluxo de electrões será muito mais intenso que o fluxo de lacunas (figura 16A e 1613), porque o número de electrões livres (portadores majoritários) é muito maior que o número de lacunas livres (portadores minoritários). Entretanto, num cristal tipo P, onde o número de lacunas (portadores majoritários) á maior que o número de electrões livres (portadores minoritários), o fluxo de lacunas será muito mais intenso que o de electrões livres (figuras 16C e 16D).
Figura 16 - Movimento dos electrões e das lacunas nos semicondutores
Em ambos os casos, á evidente que a corrente eléctrica 1, pelo circuito eléctrico, será formada apenas por electrões. Na realidade, um fluxo de lacunas da direita para a esquerda equivale a um fluxo de electrões da esquerda para a direita, do mesmo modo que um fluxo de lacunas da esquerda para a direita cor responde a um fluxo de electrões da direita para a esquerda. Desta forma, as correntes de lacunas e electrões somam-se no interior do cristal, produzindo a corrente externa 1.
COMBINAÇÃO DE IMPUREZAS DOADORAS E ACEITADORAS
Tabela 4 |
|
| Cristal tipo N | Cristal tipo P |
| Impurezas: Doadoras | Impurezas: Aceitadoras |
| Átomos Pentavalentes: As, P, Sb | Átomos Trivalentes: Al, B, Ga, In |
| Portadores Majoritários: Electrões | Portadores Majoritários: Lacunas |
| Portadores Minoritários: Lacunas | Portadores Minoritários: Electrões |
À medida que as impurezas aceitadoras são introduzidas no cristal tipo N, a resistividade do material aumenta, pois os electrões livres do cristal vão preenchendo as lacunas provocadas por estas impurezas. Quando o número de átomos trivalentes adicionados for igual ao número de átomos pentavalentes do cristal, a resistividade do semicondutor será a máxima possível. Se continuarmos introduzindo impurezas aceitadoras, o número de átomos trivalentes irá exceder o número de átomos pentavalentes, fazendo com que a resistividade do semicondutor diminua. A partir deste momento ele se transforma em um cristal tipo P, pois o número de lacunas será maior que o de electrões livres.
O mesmo efeito ocorre quando adicionamos impurezas doadoras num cristal tipo P, permitindo concluir que é possível transformar um cristal N em um cristal P, e vice-versa, sem a necessidade de realizar uma nova purificação.
A RESISTIVIDADE DOS SEMICONDUTORES DOPADOS
A resistividade dos cristais puros (intrínsecos) diminui à medida que a temperatura aumenta, o mesmo ocorrendo nos cristais dopados (tipos N e P). Contudo, a resistividade desses cristais é afectada sensivelmente pelas impurezas que lhe são adicionadas.
Como exemplo, tomemos um pedaço de 1 cm3 de Germânio puro, e se ele apresentar na temperatura ambiente uma resistência eléctrica da ordem de 50W, esse mesmo pedaço de Germânio, quando tratado com impurezas doadoras, isto é
, transformado num cristal tipo N, terá uma resistência eléctrica próxima a 2W.
Resumo
1 - Todas as substâncias encontradas na natureza são um aglomerado de moléculas,
constituídas por átomos. Estes por sua vez, são formados por três tipos de
partículas elementares:
os electrões
os protões
os neutrões
2 - Os protões e os neutrões constituem o núcleo do átomo; os electrões giram em redor do núcleo.
3 - Os protões possuem carga eléctrica positiva (+); os electrões, carga eléctrica negativa (-); e os neutrões, carga eléctrica neutra (ou nula).
4 - Os electrões que giram em torno do núcleo distribuem-se em várias regiões ou camadas, sendo a mais externa a camada de valência. Os electrões dessa camada recebem o nome de electrões de valência e são eles que, geralmente, participam das reacções químicas e dos fenómenos eléctricos.
5 - Ião negativo é todo o átomo que ganhou um ou mais electrões. Ião positivo é todo o átomo que perdeu um ou mais electrões.
6 - As substâncias encontradas na natureza são classificadas em três grupos:
condutores
isolantes
semicondutores
7 - A grandeza eléctrica usada para diferenciar os diversos materiais é chamada de resistividade.
8 - Os condutores possuem uma resistividade muito baixa, enquanto que a dos isolantes é muito elevada. Os semicondutores comportam-se de um modo intermédio, conduzindo mais corrente eléctrica que os isolantes, porém menos que os condutores.
9 - A resistividade dos condutores aumenta quando a temperatura aumenta e a dos
semicondutores diminui quando a temperatura aumenta.
10 - O Germânio e o Silício possuem uma estrutura cristalina, onde os seus átomos estão unidos por ligações covalentes.
11 - Quando uma ligação covalente é rompida e um electrão abandona, no lugar desse electrão passa a haver uma lacuna (ausência de electrão).
12 - Quando um electrão preenche o lugar de uma lacuna, completando a ligação covalente, dizemos que houve uma recombinação.
13 - A produção de pares electrões-lacunas, pelo calor, denomina-se geração térmica de portadores. Quanto maior a temperatura, maior será o número de electrões e lacunas livres no cristal do semicondutor.
14 - Os átomos diferentes do silício e
do germânio, adicionados num cristal semicondutor, chamam-se impurezas. O
processo pelo qual esses átomos são introduzidos no cristal denomina-se
dopagem.
15 - Semicondutor intrínseco é um cristal puro. Semicondutor extrínseco é um
cristal impuro ou dopado.
16 - Os átomos pentavalentes, como o Fósforo (P), o Antimônio (Sb) e o arsênio (As) são impurezas doadoras. Esses átomos possuem 5 electrões de valência.
17 - Os átomos trivalentes, como o alumínio (Al), o boro (B), o gálio (Ga) e o índio (In)são impurezas aceitadoras. esses átomos possuem 3 electrões de valência.
18 - Cristal semicondutor tipo N é todo o cristal dopado com impurezas doadoras.
19 - Cristal semicondutor tipo P é todo o cristal dopado com impurezas aceitadoras.
20 - Num cristal tipo N, os electrões são portadores majoritários, pois estão em maioria e as lacunas são portadores maioritários, porque constituem a minoria.
21 - Num cristal tipo P, as lacunas são portadores majoritários e os electrões portadores minoritários.
22 - Quando um cristal semicondutor é submetido a uma diferença de potencial (ou tensão eléctrica), as lacunas movimentam-se em sentido contrário ao dos electrões.
|
|
||
|
|
||
Os artigos são da responsabilidade de quem os escreveu. Os restantes conteúdos de - © Radioamadores.net |
||
| Página "Semicondutores" actualizada em: 01-04-2008 | ||
| |Home Page | | ||